Mistura de soluções de mesmo soluto

Uma solução é uma mistura homogênea (apresenta uma única fase/ aspecto visual), na qual temos a presença de um material (soluto) dissolvido em outro (solvente). Um exemplo de solução é a adição do cloreto de sódio (NaCl) à água (H2O).
É muito comum prepararmos soluções no dia a dia, bem como realizarmos a mistura de uma com outra. Misturar duas soluções é o ato de colocar duas ou mais soluções em um mesmo recipiente. Se essa mistura envolver soluções que apresentam o mesmo solvente e o mesmo soluto, a realização desse procedimento será chamada de mistura de soluções de mesmo soluto.
Um exemplo de mistura de soluções de mesmo soluto é quando colocamos duas soluções aquosas (apresentam água como solvente) de cloreto de sódio em um mesmo recipiente, como representado a seguir:
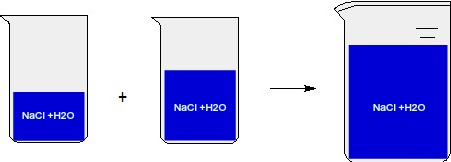
Representação de uma mistura de soluções de mesmo soluto
Analisando a imagem, podemos observar que, quando realizamos uma mistura de soluções que apresentam o mesmo soluto e o mesmo solvente, estamos apenas realizando um aumento da quantidade do solvente e do soluto, não sendo observada nenhuma outra modificação.
Na representação a seguir, temos a indicação da quantidade de soluto e solvente em cada recipiente. Observe o resultado final dessa mistura:
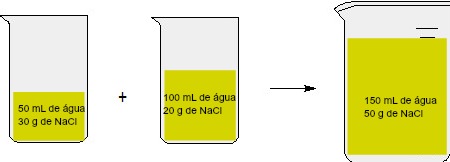
Representação de uma mistura de soluções de mesmo soluto com valores
Observa-se que a primeira solução apresentava 50 mL de solvente e 30 gramas de soluto, enquanto a segunda apresentava 100 mL de solvente e 20 gramas de soluto. Ao misturar as duas, o volume resultante foi de 150 mL e a quantidade de NaCl passou a ser 50 gramas.
Dessa forma, podemos afirmar que, quando realizamos uma mistura de soluções que apresentam o mesmo soluto e o mesmo solvente, vamos ter como resultado uma soma dos volumes das soluções misturadas e uma soma das massas (quantidades) dos solutos misturados.
Volume final = volume da solução 1 + volume da solução 2
Massa do soluto final = massa do soluto da solução 1 + massa do soluto da solução 2
Por meio desses dados, é possível realizar ainda o cálculo da concentração tanto das soluções que serão misturadas (soluções iniciais) quanto da solução resultante da mistura (solução final). As modalidades de concentração mais utilizadas são a concentração comum e a molaridade, que apresentam as seguintes fórmulas:
-
Concentração comum
C = m1
V
C = concentração comum;
V = volume da solução;
m1 = massa do soluto.
Exemplo: Uma solução de 200 mL com 20g de NaCl é misturada com outra de 400 mL e 80 g de NaCl. Quais são as concentrações comuns dessas soluções?
|
m1 = 20g C1 = 20 C1 = 0,1 g/mL |
m1 = 80g C2 = 80 C1 = 0,2 g/mL |
-
Molaridade
M = m1
M1.V
M = Molaridade;
V = volume da solução (em Litro);
M1 = massa molar do soluto.
Para calcular a molaridade de duas soluções que foram misturadas, basta utilizar a fórmula da molaridade (transformando o volume fornecido de mL para litros e dividindo por 1000) para cada solução da seguinte maneira:
|
m1 = 20g M1 = 20 M1 = 20 M1 = 1,70 mol/L |
m1 = 80g M2 = 80 M2 = 80 M2 = 3,41 mol/L |
Para calcular a concentração comum da solução final a partir das concentrações e volumes fornecidos por um exercício, utilizamos a seguinte fórmula:
C1.V1 + C2.V2 = CF.VF
C1= Concentração da solução 1;
C2= Concentração da solução 2;
CF= Concentração da solução final;
V1= Volume da solução 1;
V2= Volume da solução 2;
VF= Volume da solução final.
Já para calcular a molaridade da solução final a partir das concentrações e volumes fornecidos por um exercício, utilizamos a seguinte fórmula:
M1.V1 + M2.V2 = MF.VF
M1= Molaridade da solução 1;
M2= Molaridade da solução 2;
MF = Molaridade da solução final.
Agora veremos exemplos de cálculos envolvendo as misturas de soluções de mesmo soluto:
Qual é a molaridade de uma solução de NaOH formada pela mistura de 60 mL de solução 5 mol/L com 300 mL de solução 2 mol/L de mesma base?
Passo 1: Dados do enunciado
V1 = 60 mL
M1 = 5 mol/L
V2 = 300 mL
M2 = 2 mol/L
Passo 2: O volume da solução final é determinado pela soma dos volumes das duas soluções:
VF = V1 + V2
VF = 60 + 300
VF = 360 mL
Passo 3: A concentração da solução final após a mistura será determinada por meio dos dados na seguinte fórmula:
5.60 + 2.300 = MF.360
300 + 600 = MF.360
900 = MF.360
900 = MF
360
MF = 2,5 mol/L
Observação: Um detalhe importante é o de que a concentração da solução final após uma mistura de soluções de mesmo soluto sempre terá um valor intermediário em relação ao das soluções que foram misturadas. O exemplo acima nos mostra exatamente esse fato.
Qual será o volume de uma solução de hidróxido de sódio 60 g/L que deve ser misturado a 300 mL de uma solução 80g/L de mesma base a fim de torná-la uma solução 72 g/L?
Passo 1: dados do enunciado
V1 = ?
C1 = 60g/L
V2 = 300 mL
C2 = 80 g/L
CF = 72 g/L
Passo 2: O volume final é determinado pela soma dos volumes das duas soluções:
VF = V1 + V2
VF = V1+ 300
Passo 3: O cálculo do volume da solução 1 será feito por meio da fórmula a seguir. Mas, atenção: o VF será substituído por V1 + 300
60.V1 + 80.300 = 72.(V1 +300)
60V1 + 24000 = 72V1 + 21600
24000 – 21600 = 72V1 + 60V1
2400 = 12V1
2400 = V1
12
V1 = 200 mL
Artigos Relacionados

Últimas notícias
Outras matérias


















