Ligação covalente dativa
Ligação covalente dativa ocorre quando um átomo compartilha seus elétrons. Essa ligação obedece à Teoria do Octeto, onde os átomos se unem tentando adquirir oito elétrons na camada de valência para atingir a estabilidade eletrônica.
Exemplo: formação de dióxido de enxofre (SO2).
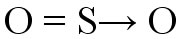
O átomo de enxofre (S) adquire seu octeto através da ligação com o oxigênio localizado à esquerda (ligação dupla coordenada). O oxigênio à direita necessita de elétrons para completar a camada de valência, e então o enxofre doa um par de elétrons para esse oxigênio. Essa transferência de elétrons é indicada pelo vetor (seta) e corresponde à ligação covalente dativa.
Vejamos o compartilhamento de elétrons na formação do composto Sulfato, onde um átomo central de enxofre estabelece ligações covalentes com quatro átomos de oxigênio.
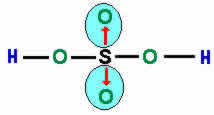
As setas vermelhas indicam as ligações dativas e os traços indicam o compartilhamento de elétrons. Na ligação dativa, o átomo de enxofre "doa" um par de elétrons para cada átomo de oxigênio, estes, por sua vez, atingem a estabilidade eletrônica.
Veja mais!
Ligação metálica
Ligação iônica
Artigos Relacionados

Últimas notícias
Outras matérias


















