Leis Ponderais

No século XVIII, houve um grande avanço do estabelecimento da Química como uma ciência bem fundamentada e os cientistas passaram a adotar o “método científico” em seus estudos. Por meio de estudos meticulosos e experiências cuidadosas, foram introduzidas leis importantes que conseguiram explicar como as reações químicas ocorrem e como as substâncias se comportam com uma regularidade de modo geral.
Entre essas leis estavam as leis ponderais, que eram aquelas que relacionavam as massas dos participantes de uma reação química.
As leis ponderais mais importantes foram duas:
1. Lei de Conservação das Massas ou Lei de Lavoisier:
Essa lei foi criada por Antoine Laurent Lavoisier (1743-1794) e disse que:
“Em uma reação química feita em recipiente fechado, a soma das massas dos reagentes é igual à soma das massas dos produtos.”
Atualmente, essa lei é mais conhecida pelo seguinte enunciado:
“Na natureza nada se cria, nada se forma, tudo se transforma.”
Lavoisier chegou a essa conclusão porque ele realizou várias reações químicas e pesou cuidadosamente as massas das substâncias envolvidas no início e no final de cada reação. Por exemplo, uma das reações que ele realizou foi a combustão do mercúrio metálico, produzindo óxido de mercúrio II:
Mercúrio metálico + oxigênio → óxido de mercúrio II
100,5 g 8,0 g 108,5 g
Observe que a soma das massas dos dois reagentes é exatamente igual à massa do produto. Lavoisier verificou experimentalmente que esse fato acontecia com regularidade, sem restrições e, por isso, criou a lei de conservação das massas citada.
2. Lei das Proporções Constantes ou Lei de Proust:
Essa lei foi criada por Joseph Louis Proust (1754-1826) e pode ser enunciada assim:
“A proporção em massa das substâncias que reagem e que são produzidas numa reação é fixa, constante e invariável.”
Por exemplo, ao se passar uma corrente contínua na água (eletrólise), ela é decomposta em seus constituintes: hidrogênio e oxigênio. Os dados experimentais mostram que as massas dessas duas substâncias sempre estarão na mesma proporção de 1:8, como mostram os exemplos abaixo:
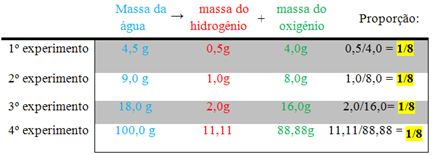
Isso ocorre em todas as reações químicas, as massas das substâncias reagem sempre numa mesma proporção.

Últimas notícias
Outras matérias


















