Equilíbrio iônico da água

A água é uma substância anfótera, ou seja, em determinadas situações, ela comporta-se como ácido e, em outras, como base. Segundo a teoria ácido-base de Brönsted-Lowry, um ácido é toda substância que doa prótons (o termo “prótons” é usado em referência ao cátion hidrogênio, H+), e as as bases são as substâncias que recebem prótons.
Assim, conforme pode ser observado a seguir, uma molécula de água pode atuar como ácido, doando um de seus prótons para outra molécula de água, que, por sua vez, atuará como base.
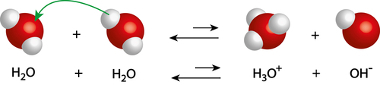
Ilustração de autoionização da água
Veja que a molécula que recebeu o próton (base) forma o cátion hidrônio (H3O+), que é o ácido conjugado, e a que perdeu o próton (ácido) forma o ânion hidróxido (OH-), que é a base conjugada. Isso significa que ocorreu uma autoionização da água. A equação mostrada acima nos mostra o equilíbrio iônico da água.
Esse equilíbrio pode também ser expresso de forma mais simplificada assim:
H2O(l) ↔ H+(aq) + OH-(aq)
No entanto, a água é um eletrólito fraco, ou seja, o seu grau de ionização (α) é muito pequeno e, consequentemente, a sua constante de ionização em termos de quantidade de matéria (KC) também é pequena. Isso é comprovado quando se testa a condutividade elétrica da água pura (água destilada), que é realmente muito baixa.
Por meio dessas medidas de condutividade elétrica experimentais, determinou-se que, a 25 ºC, a concentração desses íons na água é igual a 1 . 10-7 mol. L-1. Isso significa que a cada 1 bilhão (1 000 000 000 ou 109) de moléculas de água, apenas duas sofrem a ionização que mencionamos. Por isso a água é um eletrólito tão fraco.
Esse fato indica que o equilíbrio iônico da água está deslocado no sentido inverso, ou seja, para a esquerda, no sentido de formação das moléculas de H2O. Isso é indicado pela seta dupla na representação mais acima.
Todo equilíbrio apresenta uma constante de equilíbrio Kc, cuja expressão, conforme mostrado no texto Constante de Equilíbrio, é dada por:
Denominador: multiplicação das concentrações dos produtos da equação elevadas aos expoentes, que são iguais aos respectivos coeficientes das substâncias na equação química;
Numerador: multiplicação das concentrações dos reagentes da equação elevadas aos expoentes, que são iguais aos respectivos coeficientes das substâncias na equação química.
A expressão da constante de ionização ou da constante de dissociação iônica, Ki, é feita da mesma forma, com a única diferença de que possui íons. Assim, para o equilíbrio iônico da água, temos a seguinte expressão da sua constante de dissociação iônica Ki:
2 H2O(l) ↔ H3O+(aq) + OH-(aq) ou H2O(l) ↔ H+(aq) + OH-(aq)
Ki = [H3O+] . [OH-] ou Ki = [H+] . [OH-]
[H2O]2 [H2O]
Porém, é necessário lembrar que as substâncias sólidas e líquidas não são colocadas na expressão de Kc porque as concentrações em quantidade de matéria não podem sofrer variação nesses sistemas. Participam dessa expressão somente os sistemas gasosos e em soluções aquosas. Por isso, a concentração das moléculas de água não é escrita no numerador. Desse modo, a expressão fica assim:
Ki = [H3O+]. [OH-] ou Ki = [H+]. [OH-]
Como se trata do equilíbrio iônico da água, costuma-se substituir a constante de dissociação iônica Ki por KW, em que “w” vem de water, que é água em inglês. A constante KW é chamada de constante de dissociação da água, de constante autoprotólise ou, principalmente, de produto iônico da água.
Kw = [H+]. [OH-]
Na equação mostrada mais acima, que representa o equilíbrio iônico da água, vimos que a quantidade de íons H3O+e OH- formados é igual e na mesma proporção de 1 : 1. Então, a concentração desses dois íons na água destilada a 25ºC é a mesma, isto é, igual a 1 . 10-7 mol. L-1. Desse modo, temos:
Kw = [H+]. [OH-]
Kw = (1 . 10-7 mol. L-1) . (1 . 10-7 mol. L-1)
Kw = 1 . 10-14 (mol. L-1)2
Isso lembra o conceito de pH (potencial hidrogeniônico), que é definido como o logaritmo negativo da concentração de íons H+ na base 10:
colog [H+] = - log [H+]
pH = - log [H+]
[H+] = 10-pH
Visto que para a água temos [H+] = 10-7 a 25ºC, então, o pH da água é igual a 7. Veja:
pH = - log [H+]
pH = - log 10-7
pH = 7
O mesmo se aplica ao pOH, que também é igual a 7, mostrando, assim, que a água destilada é neutra.

A água destilada é neutra a 25ºC, com pH igual a 7
Mas os valores de KW variam com a temperatura. Observe por meio dos valores fornecidos na tabela a seguir que as concentrações dos íons H3O+e OH- em água aumentam com o aumento da temperatura. Consequentemente, o valor do KW também aumenta:

Tabela de produto iônico da água em diferentes temperaturas
Assim, o valor de KW da água no estado de vapor é maior que o da água líquida, que, por sua vez, é maior que o do gelo.
Artigos Relacionados

Últimas notícias
Outras matérias


















