Eletroquímica

A Eletroquímica é um ramo da Química que estuda o fenômeno da transferência de elétrons para a transformação de energia química em energia elétrica e vice-versa.
As reações que envolvem transferência de elétrons são chamadas de reações de oxirredução, pois nelas ocorrem simultaneamente a redução e a oxidação. A espécie química que perde elétrons passa por uma oxidação e fica com o Nox (número de oxidação) maior. Já a espécie química que recebe esses elétrons passa por uma redução e o seu Nox fica menor.
Por exemplo, a seguir há uma reação desse tipo, na qual uma placa de zinco metálico (Zn0) é colocada em uma solução de sulfato de cobre (que possui cátions cobre II (Cu2+) dissolvidos). O zinco sofre oxidação, perdendo dois elétrons e transformando-se no cátion zinco (Zn2+), enquanto os íons cobre recebem esses elétrons e transformam-se em cobre metálico (Cu0). Veja a equação iônica desse processo:
Zn(s) + Cu2+(aq) → Zn2+(aq) + Cu(s)
Assim, nos fenômenos eletroquímicos, sempre ocorrem reações semelhantes a essa. Porém, isso pode ocorrer de duas formas. Os dois campos de estudo principais da Eletroquímica são:
* Pilhas e baterias: Nesse caso existe a conversão de energia química em energia elétrica, ou seja, usam-se as reações químicas de oxirredução espontâneas para a geração de eletricidade.
Dentro das pilhas são colocadas certas substâncias químicas que reagem espontaneamente transferindo elétrons, isto é, por meio de reações de oxirredução. As pilhas possuem dois eletrodos, que são:
- ânodo: polo negativo onde ocorre a oxidação;
- cátodo: polo positivo onde ocorre a redução.
As pilhas e baterias também possuem um eletrólito, que é uma solução condutora de íons. Assim, forma-se um fluxo de elétrons entre esses polos que resulta na formação de uma corrente elétrica que pode ser utilizada para que diversos aparelhos elétricos funcionem.
A diferença entre as pilhas e as baterias é que enquanto as pilhas possuem somente dois eletrodos, as baterias são formadas por várias pilhas conectadas em série ou em paralelo, ou seja, possuem vários eletrodos, o que aumenta a sua voltagem.
O que seria de nossa sociedade sem as pilhas e as baterias que fazem funcionar os celulares, os carros, os relógios e muitos outros aparelhos?

Exemplos de baterias (de celulares e de automóveis) usadas no cotidiano
* Eletrólise: É o processo inverso que ocorre nas pilhas e baterias, ou seja, ocorre a transformação de energia elétrica em energia química. Utiliza-se energia elétrica para forçar a ocorrência de uma reação química não espontânea pela neutralização das cargas dos íons e formação de substâncias simples.
Isso ocorre quando se passa uma corrente elétrica proveniente de algum gerador (como uma pilha ou uma bateria) por um líquido iônico (substância fundida - eletrólise ígnea) ou por uma solução aquosa que contém íons (eletrólise em meio aquoso). Desse modo, o cátion presente no líquido ou na solução recebe elétrons, e o ânion doa elétrons, para que ambos fiquem com carga elétrica igual a zero e com energia química acumulada.
A eletrólise é usada para a produção de substâncias simples de uso importante que não são encontradas na natureza, como o gás cloro e o sódio metálico produzidos na eletrólise ígnea do cloreto de sódio. Na eletrólise aquosa do cloreto de sódio, além de o cloro ser produzido, também se obtém o gás hidrogênio que é usado como combustível. Mais detalhes sobre como ocorrem esses processos podem ser vistos no texto Eletrólise do cloreto de sódio.
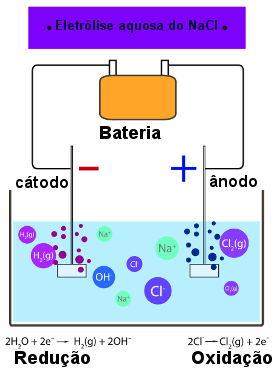
Eletrólise aquosa do cloreto de sódio com produção de cloro e hidrogênio
A eletrólise também é usada para a produção de metais, como mostra o artigo Produção de alumínio por eletrólise, e para o desenvolvimento de processos de proteção de metais contra a corrosão.
A Eletroquímica é, portanto, um ramo muito importante não só porque está relacionada com o desenvolvimento tecnológico e de métodos de produção de eletricidade, mas também porque permite inclusive a monitoração das atividades do cérebro e do coração, do pH do sangue, da presença de contaminantes na água, além de possibilitar a criação de equipamentos que salvam vidas, como o marcapasso, e assim por diante.
Artigos Relacionados

Últimas notícias
Outras matérias


















