Transformação isobárica

Certa quantidade de gás sofre uma transformação de estado quando se modificam ao menos duas das variáveis de estado (temperatura, volume e pressão). Nosso objeto de estudo são as transformações em que uma das variáveis se mantém constante, variando, portanto, as outras duas.
Uma transformação gasosa na qual o volume (V) e a temperatura (T) variam e a pressão (p) permanece constante recebe a denominação de transformação isobárica. Dois físicos, Charles e Gay-Lussac, estabeleceram através de experimentos a seguinte relação:
Mantendo-se um gás ideal sob pressão constante, seu volume aumenta com o aumento da temperatura.
No gráfico abaixo podemos verificar a variação do volume em função da temperatura (em graus Celsius) de um determinado gás ideal, mantendo a pressão constante. A fim de expressar a relação quantitativa entre volume e a temperatura podemos fazer uso da equação da dilatação volumétrica:
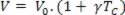
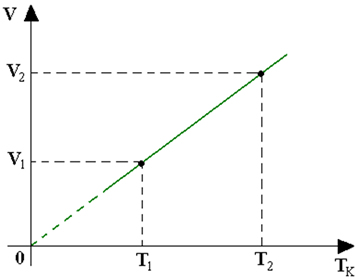
Na equação acima o volume inicial (V0) representa o volume do gás à temperatura de 0ºC, (V) volume do gás à temperatura (TC) em graus Celsius e γ é o coeficiente de dilatação dos gases cujo valor é 1/273 ºC-1. Dessa forma, podemos expressar a transformação isobárica da seguinte maneira:
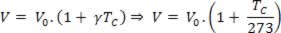
Como TC = TK – 273, temos:
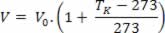
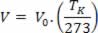
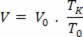
Nessa última equação, T0 = 273 K, ou seja, 0ºC. De tal modo, podemos estabelecer que, na transformação isobárica, o volume do gás ideal é proporcional à temperatura, portanto a equação acima fica:
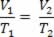
Artigos Relacionados

Últimas notícias
Outras matérias


















