Dilatação dos gases

Muito raramente vemos um balão voando. Mas em algumas cidades o voo em balões ocorre com bastante frequência. É interessante ressaltar a física envolvida no funcionamento desse equipamento. Quando o baloeiro acende a chama da tocha do balão, ele faz com que o ar interno se dilate, enchendo o balão. Podemos dizer que as moléculas no ar aquecido têm maior energia cinética, portanto elas se chocam, com mais intensidade, com as paredes do balão, pressionando-as de dentro para fora.
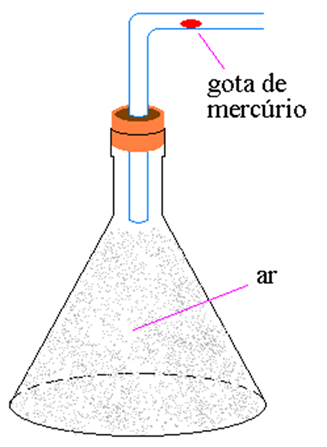
Vejamos a figura abaixo: nela temos um recipiente fechado somente com ar em seu interior. Ao ser aquecido, o ar interno se expande e ao mesmo tempo empurra uma pequena gota de mercúrio que está contida no tubo horizontal. Como sabemos, quando aquecido, o ar se dilata e ocupa um volume maior. Nesse caso, supondo que o processo seja lento, podemos considerar que o ar dilata-se à pressão constante.
Se tivéssemos como medir a dilatação do ar no exemplo citado anteriormente, veríamos que ela confirma com exatidão a lei da dilatação dos sólidos e líquidos, porém apresentaria apenas uma simples diferença: que, diferentemente dos sólidos e dos líquidos, no caso dos gases, o coeficiente de dilatação volumétrica é igual para qualquer tipo de gás. De acordo com a teoria cinético-molecular, esse fenômeno ocorre pelo fato de não haver interação entre as moléculas de um gás. Já nos sólidos e líquidos, há interação molecular, que é diferente para cada substância.
Sendo assim, podemos dizer que o coeficiente de dilatação volumétrica dos gases indica que o volume de um gás, à temperatura inicial 0ºC, diminui 1/273 quando sua temperatura é reduzida em 1ºC. Diminuindo-se a temperatura em 10ºC, o volume diminuiria 10/273. Se a temperatura do gás atingisse 273ºC, isto é, fosse de 0ºC para -273ºC, seu volume diminuiria 273/273, teoricamente, seria reduzido a zero.
Na prática, porém, os gases passam para o estado líquido antes de atingirem a temperatura -273ºC. Essa temperatura representa a condição teórica de contração máxima possível, na qual a energia cinética das moléculas seria mínima: é o zero absoluto na escala Kelvin e, teoricamente, a menor temperatura que se pode atingir.
Artigos Relacionados

Últimas notícias
Outras matérias


















